

| French
|
Arabic
|
English
|
| Enzymes allostériques, Enzymes régulatrices | إنزيمات الموقع الآخر، إنزيمات ألوستيرية، إنزيمات منظمة | Allosteric enzymes, Regulatory enzymes |
Allosteric enzymes (إنزيمات منظمة) are enzymes involved in the regulation of metabolic chains. They change their conformation upon binding of an effector (allosteric inhibitor or allosteric activator). This conformation change induces an apparent change in binding affinity at a different ligand binding site. Allostery (ألوستيرية) plays a crucial role in many fundamental biological processes, including the regulation of metabolism.
تلقب الإنزيمات المنظمة (regulatory Enzymes, Enzymes régulatrices) التي تساهم في تنظيم المسارات الأيضية (Chaînes métaboliques) بالإنزيمات ذات الموقع الآخر أو الإنزيمات الألوستيرية (allosteric enzymes, Enzymes allostériques) وذلك لكون الإنزيم يتوفر على نوعين من المواقع، منها الموقع النشيط (active site, Site actif) الذي ترتبط به الركيزة (Substrate, Substrat) و الموقع المنظم أو الموقع الألوستيري (regulatory site, allosteric site, Site régulateur, site allostérique) الذي يستقبل العنصر المحفز على التنظيم والذي يكون مثبطا يدعى 'مثبط ألوستيري' (allosteric inhibitor, Inhibiteur allostérique) أو منشطا يلقب ب'منشط ألوستيري' (allosteric activator, Activateur allostérique). إقترح إسم 'الإنزيمات ذات الموقع الآخر' (الإنزيمات الألوستيرية) في إطار دراسة التثبيط التنافسي الذي يحدثه الناتج الأخير في المسارات الأيضية (competitive inhibition of the metabolic pathways by the end product, Inhibition compétitive par le produit final des chaînes métaboliques)، علما أن بنية الناتج الأخير تختلف عن بنية الركيزة. آنذاك، وضع السؤال 'كيف لمركب مختلف البنية مع الركيزة، أن يكون مثبطا تنافسيا لهذه الأخيرة ؟'. ثبت فيما بعد أن التثبيط يتم بارتباط الناتج الأخير بموقع آخر بعيد عن الموقع النشيط ليحدث تغيرا بنيويا ينعكس على شكل الموقع النشيط الذي يصبح عاجزا عن ربط مادة الساس (أنظر الرسم الموالي).
في معظم أنظمة متعددة الإنزيم (multienzymatic enzymes) يكون الإنزيم الأول في السلسلة منظما لسرعة النظام ككل ويسمى هذا الإنزيم بالإنزيم المنظم أو الإنزيم الألوستيري، الذي يخضع عادة للتثبيط الرجعي (feedback inhibition) بالناتج النهائي للسلسلة (Final product of the chain)

هكذا عندما يتجمع الناتج النهائي إلى تركيز ع ا ل ي، يقوم نفسه بتثبيط أول إنزيم في المسار الأيضي أي الذي يحفز التفاعل الأول في السلسلة و الذي غالبا ما يكون الإنزيم المنظم في السلسلة (أنظر الرسم).
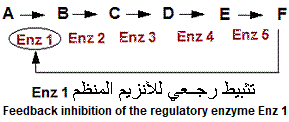
هكذا، يتوقف عمل السلسلة من استكمال تفاعلاتها الحيوية
للإنزيمات
المنظمة صفات متعددة، تميزها عن الإنزيمات غير المنظمة (الخاضعة لحركية ميكايلس)
و يتجلى ذلك على جوانب البنية و الحركية.
- ظهور الحركية السينية (sigmoidal kinetic, Cinétique sigmoïde)
و خاصية فعل التعاونية (cooperativity effect, Effet de coopérativité).
تتميز الإنزيمات المنظمة عن الإنزيمات غير المنظمة بعدة صفات، من أبرزها الحركية السينية (sigmoidal kinetic, Cinétique sigmoïde) كما
يوضحها الرسم التالي.
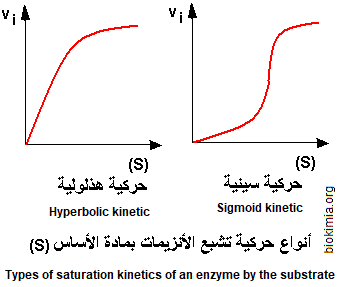
هذا
لا يعني أن كل الإنزيمات المنظمة لها نفس الحركية، بل تظهر البعض منها حركية هذلولية (hyperbolic kinetic, Cinétique hyperbolique). هكذا، إذا تتبعنا كيفية تشبع إنزيم ما بمادة التفاعل (S)، يمكن الاطلاع على التشبع الإنزيمي السيني (sigmoidal saturation, Saturation sigmoïde) و التشبع الهذلولي (hyperbolic saturation, Saturation hyperbolique) برسم منحنيات المعادلة v = f((S))، كما يوضحه الرسم.
المزيد في كتاب علوم الحياة. بروتينات و إنزيمات، م. بعزيز، 2013
يوجد العديد من الإنزيمات المنظمة ذاخل خلايا الكائنات الحية و هي تنتمي إلى سلاسل متعددة الإنزيم بمسارات أيضية مختلفة.
تمتاز البكتريا بتكوين حمض أميني أساسي بالنسبة للإنسان و ذلك انطلاقا من مواد أولية بسيطة توجد بخلايا هذه الكائنات الدقيقة. يتعلق الأمر بحمض الإزولوسين (Isoleucine, Ile, I). تقوم سلسلة متعددة الإنزيم على تحفيز تحويل الحمض الأميني، تريونين (Threonine, Thr, T) إلى Isoleucine بواسطة خمس خطوات محفزة بالإنزيمات. الإنزيم الأول في السلسلة وهو التريونين ديزاميناز(Threonine deaminase) يثبط بشدة بالإزولوسين الذي يمثل الناتج النهائي للسلسلة (أنظر الرسم التالي) ويعرف هذا النوع من التثبيط بالتثبيط الرجعي (Retroinhibition أو feedback inhibition ، بالأنجليزية).
The threonine deaminase is an allosteric enzyme that catalyses the pyridoxal-phosphate-dependent dehydrative deamination of L-threonine to ammonia and alpha-ketobutyrate (2-oxobutanoate, 2-Ketobutyric acid), respectively, in vivo. The conversion of threonine into oxobutanoate is also the first step in the pathway of threonine degradation. Threonine deaminase is a tetramer. It belongs to K system allosteric enzymes.



 |
 |
 |
 |
 |
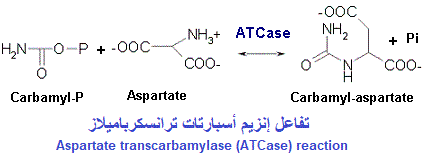
يحفز إنزيم أسبارتات ترانسكارباميلاز الذي يرمز له ب ATCase، تخليق القواعد الأزوتية البيريميدية (pyrimidic bases, Bases pyrimidiques) التي تذخل في تركبة الأحماض النووية. يتم ذلك من خلال التفاعل التالي، حيث تقدر النواتج بقياس امتصاص الضوء على موجة بطول 465 ناتومتر (أنظر الرسم التالي)
Aspartate carbamoyltransferase catalyzes the first step in the pyrimidine biosynthetic pathway. Products are evaluated by absorbance at 465 nm.
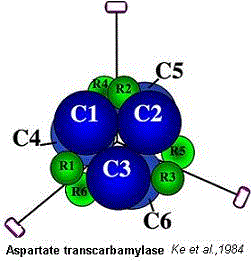
يتكون إنزيم أسبارتات ترانسكارباميلاز من تحت وحداتين مختلفتين سميتا C (اعتبارا لوظيفة التحفيز، Catalysis) و R (اعتبارا لوظيفة التنظيم، Regulation). يقدر عدد تحت وحدة C بستة (C1 حتى C6) موجودة في شكل مركبين ثلاثيين (أنظر الرسم). عدد تحت وحدة R يساوي 6، كذلك (R1 حتى R6)، لكن الوحدات مرتبة في شكل ثلاثة مركبات ثنائية، هذه المرة
ATCase is a multi-subunit protein complex composed of 12 subunits (300 kDa in total). The composition of the subunits is C6R6, forming 2 trimers of catalytic subunits (34 kDa) and 3 dimers of regulatory subunits (17 kDa). The particular arrangement of catalytic and regulatory subunits in this enzyme affords the complex with strongly allosteric behaviour with respect to its substrates.
روابط مفيدة- Useful link: Aspartate transcarbamylase. Exam
يمثل
الرسم التالي (v = f(S)) نوع الحركية التي يمتاز
بها إنزيم ATCase وهي تتغير حسب غياب وحضور المؤثرات الألوستيرية. يعد CTP (نكليوتيد) مثبطا ألوستيريا للإنزيم، إذ كلما ارتفعت مقادير النواتج في السلسلة الأيضية إلا و تذخل ليحد من هذا بتفاعله مع الإنزيم المنظم.
العكس يقع بحضور ATP ، الذي يعتبر
منشطا ألوستيريا للأتزيم. بفقدان حساسيته، يظهر إنزيم ATCase حركية
شبيهة بحركية ميكايليس-مانتن (حركية هذلولية)

ATCase
does not follow Michaelis-Menten kinetics, but lies between the low-activity, low-affinity "tight" or T and the high-activity, high-affinity "relaxed" or R states. The binding of substrate to the catalytic subunits results in an equilibrium shift towards the R state, whereas binding of CTP to the regulatory subunits results in an equilibrium shift towards the T state. CTP is an allosteric inhibitor.
Binding of ATP to the regulatory subunits results in an equilibrium shift towards the R state. ATP is an allosteric activator.
سؤال 1 - Q1
اختر المعلومة الخاطئة المتعلقة بالإنزيمات الألوستيرية - Choose the false information relating to allosteric enzymes
(!الإنزيمات الألوستيرية هي إنزيمات لها "موقع آخر"
Allosteric enzymes are enzymes with an 'other site')(! في الإنزيمات الألوستيرية، تسمى المستقلبات التنظيمية المستجيب أو المغير
In allosteric enzymes, regulatory metabolites are called effector or modulator )( الإنزيمات الألوستيرية تعني الإنزيمات التي يكون لكل منها وظيفة متطابقة ولكنها تظهر بنية مختلفة
Allosteric enzymes are enzymes where each of them have identical function but they show different structure)
سؤال 2 - Q2
اختر المعلومة الصحيحة حول الإنزيمات الألوستيرية - Choose the true information relating to allosteric enzymes
(يمكن لبعض الإنزيمات الألوستيرية إظهار حركية مايكلية بوجود الركيزة S
Certain allosteric enzymes can show Michaelian kinetics in the presence of the substrate S)(!لا تحتاج الإنزيمات الألوستيرية إلى عوامل مساعدة، فهي تستخدم المؤثرات
الألوستيرية
Allosteric enzymes do not need cofactors, they use allosteric effectors)
سؤال 3 - Q3
اختر المعلومة الخاطئة حول الإنزيمات الألوستيرية
Choosing the false information About Allosteric Enzymes
(!غالبًا ما تحفز الإنزيمات الألوستيرية مرحلة أساسية في المسار الأيضي
Allosteric enzymes very often catalyze an essential step in a metabolic pathway)(!تحتوي الإنزيمات الألوستيرية بالضرورة على محور أو مستوى تناظر
Allosteric enzymes necessarily have an axis or plane of symmetry)(!إذا قمنا بتدمير الموقع الألوستيري للإنزيم - فقط - فإن هذا الإنزيم سوف يتصرف مثل الإنزيم الكلاسيكي الذي يتبع نموذج مايكل.
If we destroy the allosteric site of an enzyme - and only this site -, this enzyme will behave like a classic enzyme following the Michaelian model)(تتعلق الألوستيرية بالإنزيمات فقط، مع وجود بنية رباعية
Allostery concerns only enzymes, and implies a quaternary structure)
سؤال 4 - Q4
أي من الجزيئات التالية لا يعد مثبطًا لإنزيم هيدروجين البيروفات الذي يحول البيروفات إلى أسيتيل CoA؟ - Which of the following molecules is not an inhibitor of pyruvate dehydrogenase that converts pyruvate to acetyl CoA?
(الحمض الليموني - Citric acid)(! NADH)(!ATP)(!Acetyl CoA)
Q1:"إنزيمات ذات وظيفة متطابقة ولكن بنية مختلفة" هذه العبارة غير صحيحة بالنسبة للإنزيمات الألوستيرية لأنها تحدد الأشباه الإنزيمية وليس الإنزيمات الألوستيرية
“enzymes with identical function but a different structure” This statement is false for allosteric enzymes as it is defining isoenzymes and not allosteric enzymes.
Q4:Allosteric inhibitors of pyruvate dehydrogenase that converts pyruvate to acetyl CoA (and release CO2) are ATP, NADH and Acetyl CoA. Citric acid (citrate) acts as an allosteric activator for acetyl CoA carboxylase in fatty acid synthesis
المثبطات الألوستيرية لأنزيم هيدروجيناز البيروفات الذي يحول البيروفات إلى أسيتيل CoA (ويطلق ثاني أكسيد الكربون) هي ATP وNADH وAcetyl CoA. يحدث تفاعل فصم الكربون من حمض البيروفيك داخل الميتوكندري بواسطة أنزيم بيروفات ديهيدروجيناز (Pyruvate dehydrogenase) الموجود بماتريس (Matrice) الميتوكندري وفق التفاعل الغير
- Enzymologie-enzymes allostériques (Fr)
- Enzymes allostériques. Exercices
- Régulation enzymatique du métabolisme - التنظيم الأنزيمي للاستقلاب
- ENZYMES ALLOSTERIQUES
- إنزيمات. لائحة enzymes-enzymology-index
- الإنزيمات. تنقية وتطبيقات - Enzymes. Purification and applications
- إنزيمات. ميكانزمات التحفيز الإنزيمي
Enzymes. Catalysis mechanisms
- Catalyse enzymatique. Exercices
PASSER UN CONTROLE QCM SUR LES ENZYMES (THEORIE + PRATIQUE)
Afin d'encourager les illustrations vidéos des cours et données en biochimie, faite acquisition des livres de la préparation de la transition Secondaire-Supérieur et trouver toutes les vidéos sur les DVD accompagnant les ouvrages.